Идентификация и биохимия
Полное название: Генетический тест на полиморфизмы генов, участвующих в метаболизме фолатов.
Синонимы: Тест на MTHFR, анализ на мутации MTHFR, генетический анализ фолатного цикла, тест на фолатный метаболизм, SNP-анализ фолатного пути.
Основные гены: MTHFR (метилентетрагидрофолатредуктаза), MTR (метионинсинтаза), MTRR (метионинсинтаза-реактиватор), SHMT1 (серин-гидроксиметилтрансфераза 1), TYMS (тимидилатсинтаза), ATIC (аминоимидазол-карбоксамидтрансформилаза). Наиболее изучены полиморфизмы в гене MTHFR, особенно c.677C>T (p.Ala223Val) и c.1298A>C (p.Glu429Ala).
Молекулярная масса и форма: Анализ не измеряет белок или метаболит, а определяет наличие однонуклеотидных полиморфизмов (SNP) в ДНК. Соответственно, молекулярная масса не применима. Исследуемый материал — геномная ДНК, выделенная из периферической крови, слюны или эпителиальных клеток.
LOINC-код: LOINC-код может отличаться в зависимости от лаборатории и конкретного набора тестируемых SNP. Примерные коды: 57681-1 (MTHFR gene mutation analysis), 57682-9 (MTHFR c.677C>T DNA mutation analysis), 57683-7 (MTHFR c.1298A>C DNA mutation analysis).
SNOMED CT: 219154003 (Genetic testing for MTHFR mutation), 219155002 (Interpretation of MTHFR gene test).
Физиологическая роль
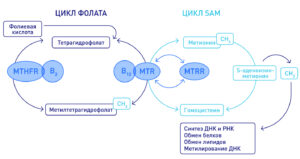
Метаболизм фолатов — ключевой биохимический путь, обеспечивающий поставку одномерных единиц (одноуглеродных фрагментов) для синтеза пуринов, тимидилата и метионина. Этот процесс необходим для репликации ДНК, реметилирования ДНК и синтеза белков.
Центральным ферментом пути является метилентетрагидрофолатредуктаза (MTHFR), кодируемая геном MTHFR. Этот фермент катализирует необратимое превращение 5,10-метилен-тетрагидрофолата в 5-метилтетрагидрофолат — основную циркулирующую форму фолата в плазме. Последний используется в реакции реметилирования гомоцистеина до метионина с участием витамина B12 и фермента метионинсинтазы (MTR).
Таким образом, активность ферментов фолатного цикла напрямую влияет на:
- Уровень гомоцистеина в крови;
- Синтез ДНК и деление клеток;
- Эпигенетическую регуляцию (через S-аденозилметионин — SAM, основной донор метильных групп);
- Нейротрансмиттерный синтез (через метилирование катехоламинов).
Путь активен в большинстве тканей, особенно в быстро делящихся (костный мозг, эпителий кишечника) и метаболически активных (печень, мозг).
Патофизиология
Полиморфизмы в генах фолатного цикла, особенно MTHFR c.677C>T и c.1298A>C, ассоциированы со снижением ферментативной активности. Гомозиготность по c.677C>T (TT-генотип) снижает активность MTHFR до 30–50% от нормы. Это приводит к:
- Гипергомоцистеинемии: из-за снижения синтеза 5-метилтетрагидрофолата, необходимого для реметилирования гомоцистеина.
- Нарушению синтеза ДНК: при дефиците тимидилата и пуринов, что может проявляться мегалобластной анемией (редко при изолированных SNP).
- Эпигенетическим нарушениям: снижение уровня SAM может нарушать метилирование ДНК и гистонов, что потенциально влияет на экспрессию генов, включая онкогены и гены-супрессоры опухолей.
Ассоциации с заболеваниями:
- Сердечно-сосудистые заболевания: умеренная гипергомоцистеинемия считается фактором риска тромбозов, инсультов и ИБС, хотя причинно-следственная связь до конца не доказана.
- Осложнения беременности: повышение риска невынашивания, преэклампсии, задержки роста плода и нейральных труб дефектов (например, спина бифида), особенно при сочетании с низким потреблением фолиевой кислоты.
- Психиатрические расстройства: слабые ассоциации с депрессией, шизофренией, аутизмом — возможно, через нарушение метилирования нейротрансмиттеров.
- Онкологические заболевания: двойственная роль: снижение активности MTHFR может снижать риск колоректального рака (за счёт лучшего сохранения 5,10-метилен-ТГФ для синтеза тимидилата), но повышать риск других опухолей.
Важно: наличие полиморфизма не означает наличие заболевания. Большинство носителей SNP MTHFR — асимптоматичны.
Референсные значения
Поскольку анализ является генетическим, нормальные значения определяются как распространённость аллелей в популяции и интерпретируются в терминах генотипа.
| Ген/Полиморфизм | Нормальный (дикого типа) генотип | Гетерозиготный вариант | Гомозиготный вариант | Комментарии |
|---|---|---|---|---|
| MTHFR c.677C>T | CC | CT | TT | TT ассоциирован с 30–50% снижением активности фермента |
| MTHFR c.1298A>C | AA | AC | CC | Снижение активности менее выражено, чем при c.677C>T |
| MTR c.2756A>G | AA | AG | GG | Вариант изучен слабее, возможна связь с гомоцистеином |
| MTRR c.66A>G | AA | AG | GG | Может усиливать эффект MTHFR при дефиците B12 |
Единицы измерения: генотип (например, CC, CT, TT). Не применяются концентрационные единицы.
Зависимость от возраста/пола: генотип стабилен с момента зачатия и не зависит от возраста, пола или состояния здоровья. Однако клиническая значимость может зависеть от возраста, питания и сопутствующих заболеваний.
Референсные значения зависят от этнической группы: частота TT-генотипа по c.677C>T варьируется от 10% в Европе до 25% в Италии и Мексике, и менее 1% в Африке.
Методы определения
Генетический тест на метаболизм фолатов проводится методами молекулярной биологии, направленными на выявление SNP.
- ПЦР в реальном времени с аллель-специфичными зондами (TaqMan): наиболее распространённый метод. Высокая чувствительность и специфичность (>99%). Платформы: ABI 7500, LightCycler. Преаналитика: ДНК из цельной крови (в EDTA), слюны или буккального мазка. Стабильность образца: ДНК стабильна при хранении при 4 °C до 7 дней, при -20 °C — годы.
- Секвенирование следующего поколения (NGS): используется при расширенных панелях (например, 5–10 генов). Позволяет выявлять редкие варианты. Требует биоинформатической обработки. Платформы: Illumina, Ion Torrent.
- Чипы SNP-генотипирования: используются в коммерческих тестах (например, 23andMe). Охватывают тысячи SNP, включая MTHFR. Могут иметь ограниченную валидацию для клинического использования.
Преаналитические требования:
- Кровь: 2–5 мл в пробирку с ЭДТА (фиолетовая крышка), избегать гемолиза.
- Слюна: стабилизаторы в наборах (например, Oragene).
- Буккальный мазок: стерильный тампон, не есть/не пить 30 мин до сбора.
Чувствительность метода: >99% для целевых SNP при использовании валидированных ПЦР-методов. Ошибки возможны при загрязнении образца или мутациях в зоне связывания праймеров.
Клинические показания
Когда назначают:
- Повторные выкидыши или привычное невынашивание беременности, особенно при нормальных иммунологических и анатомических обследованиях.
- Наличие дефектов нервной трубки у плода в анамнезе.
- Умеренная гипергомоцистеинемия (15–30 мкмоль/л), особенно при отсутствии дефицита B12 или фолата.
- Семейный анамнез тромбофилии без выявленных мутаций F5 (Лейден), F2 (протромбин).
- Планирование беременности при известном семейном анамнезе SNP MTHFR.
- Оценка индивидуальной потребности в форме фолиевой кислоты (например, L-метилфолат) у пациентов с плохой переносимостью стандартной терапии.
Когда не назначают:
- Рутинный скрининг у асимптомных пациентов без репродуктивных или тромботических осложнений.
- Диагностика депрессии, аутизма или шизофрении как монотест.
- Оценка риска сердечно-сосудистых заболеваний у пациентов без гипергомоцистеинемии.
- Перед началом терапии фолиевой кислотой у большинства пациентов — клиническая польза теста не доказана.
Интерференции и ограничения
Лекарства: препараты не влияют на результат генетического теста, так как анализируется ДНК. Однако лекарства могут влиять на уровень гомоцистеина и фолатов — это важно при интерпретации функциональных маркеров.
Биологические факторы:
- Мозаицизм (редко) может привести к ложным результатам, если мутация присутствует не во всех клетках.
- Загрязнение образца ДНК другого человека (например, при трансплантации) — может исказить результат.
Ложные результаты:
- При использовании неквалифицированных коммерческих тестов (например, на основе чипов без клинической валидации).
- Ошибки в интерпретации: например, считать гетерозиготный вариант (CT) достаточным для назначения терапии.
Ограничения теста:
- Не все полиморфизмы известны — тест может не охватывать редкие мутации.
- Наличие SNP не предсказывает уровень гомоцистеина или клинические исходы с высокой точностью.
- Эффект полиморфизмов зависит от диеты (потребление фолата, B6, B12), что не отражается в тесте.
Интерпретация и тактика
При выявлении гомозиготного (TT) или компаунд-гетерозиготного (677CT + 1298AC) генотипа:
- Оценить уровень гомоцистеина в плазме (функциональный маркер).
- Определить уровни фолиевой кислоты, витамина B12 и, при необходимости, B6.
- При гипергомоцистеинемии: начать терапию активными формами фолата — L-5-метилтетрагидрофолат (5-MTHF), 0.8–1.0 мг/сут, особенно при беременности.
- При нормальном гомоцистеине: специфическая терапия не требуется. Рекомендовать адекватное потребление фолата с пищей (зелёные овощи, бобовые) или в виде фолиевой кислоты (400 мкг/сут при планировании беременности).
Целевые значения при терапии:
- Гомоцистеин: <10–12 мкмоль/л (особенно при беременности или тромбозах).
- Фолат сыворотки: >7 нмоль/л, эритроцитарный фолат >340 нмоль/л.
Советы пациенту:
- Наличие SNP MTHFR — не диагноз, а генетическая особенность.
- Большинство людей с TT-генотипом ведут здоровый образ жизни без последствий.
- Ключевое значение имеет питание и уровень витаминов, а не сам генотип.
- Не следует назначать дорогие активные добавки без показаний (например, при нормальном гомоцистеине).
Связь с другими маркерами
Генетический тест на метаболизм фолатов интерпретируется в комплексе с биохимическими маркерами:
| Маркер | Связь | Цель одновременного определения |
|---|---|---|
| Гомоцистеин (общий, плазма) | Функциональный показатель активности фолатного цикла | Оценить, приводит ли SNP к метаболическому нарушению |
| Фолиевая кислота (сывороточная) | Субстрат для MTHFR | Выявить дефицит, усиливающий эффект SNP |
| Витамин B12 (цианокобаламин) | Кофактор метионинсинтазы | Исключить B12-дефицитную гипергомоцистеинемию |
| Витамин B6 (пиридоксальфосфат) | Кофактор цистатионин-бета-синтазы | Оценить полную картину метаболизма гомоцистеина |
| Фактор V Лейден, протромбин G20210A | Наследственные тромбофилии | Оценить суммарный генетический риск тромбозов |
Вывод
Генетический тест на метаболизм фолатов выявляет полиморфизмы в генах, участвующих в цикле одномерных фрагментов, особенно MTHFR. Наиболее значимые варианты — c.677C>T и c.1298A>C. Тест не измеряет концентрацию веществ, а определяет генотип, стабильный в течение жизни. Клиническая значимость SNP проявляется при сочетании с низким потреблением фолата, витаминов B12/B6 и проявляется гипергомоцистеинемией. Показания к тестированию — рецидивирующие выкидыши, дефекты нервной трубки, умеренная гипергомоцистеинемия. Рутинный скрининг не рекомендуется. Интерпретация требует сопоставления с уровнем гомоцистеина и витаминов. Наличие полиморфизма не является показанием к терапии без функциональных отклонений.

