Идентификация и биохимия
Полное название: Эпигенетический возраст по уровню метилирования ДНК (DNA methylation-based epigenetic age).
Синонимы: Биологический возраст, эпигенетические часы, метиломный возраст, DNAmAge, epigenetic clock, DNA methylation age.
Ген(ы): Анализ не фокусируется на одном конкретном гене. Оценивается уровень метилирования в сотнях конкретных цитозин-фосфат-гуанин (CpG) участков по всему геному. Наиболее значимые CpG-сайты включают локусы в или рядом с генами, такими как ASPA, PHOSPHO1, PDE4C, KLF14, EDARADD, ITGA2B, NT5C2, SLC12A5, ELOVL2, FHL2 — в зависимости от используемой модели (например, Horvath’s clock, Hannum’s clock, PhenoAge, GrimAge).
Молекулярная масса: Не применимо. Анализ основан на химической модификации (метилировании) цитозина в ДНК, а не на белке или метаболите с определённой молекулярной массой.
Форма: Метилированный цитозин (5-метилцитозин, 5mC) в CpG-динуклеотидах геномной ДНК, выделенной из биологических образцов (обычно цельная кровь, сыворотка, слюна, эпителий).
LOINC-код: LOINC-код может отличаться в зависимости от лаборатории и конкретной реализации теста. Некоторые лаборатории используют комбинированные коды или не имеют стандартизированного LOINC-кода. Возможные коды включают 96233-3 (DNA methylation age panel in Blood by Sequencing) или 96234-1 (DNA methylation age panel in Saliva by Sequencing), но они не универсальны.
SNOMED CT: SNOMED-коды для эпигенетического возраста не стандартизированы и варьируются. Может использоваться общий код 723134000 (Biological age measurement), но он не специфичен для метилирования ДНК.
Физиологическая роль
Метилирование ДНК — одна из ключевых эпигенетических модификаций, регулирующих экспрессию генов без изменения последовательности ДНК. Оно заключается в присоединении метильной группы (-CH₃) к цитозину в CpG-островках, преимущественно в промоторных регионах генов. Гиперметилирование промотора обычно подавляет транскрипцию, тогда как гипометилирование может активировать экспрессию.
Эпигенетические изменения, включая метилирование, играют центральную роль в:
- Клеточной дифференцировке: Во время эмбриогенеза и развития тканей метилирование помогает запирать ненужные гены.
- Поддержании геномной стабильности: Гипометилирование повторяющихся последовательностей может приводить к хромосомной нестабильности.
- Регуляции старения: С возрастом наблюдаются систематические изменения в метильном профиле: гиперметилирование некоторых генов и гипометилирование других, что ассоциируется с нарушением гомеостаза, клеточным старением (senescence) и снижением регенеративной способности.
Ключевые сигнальные пути, с которыми пересекаются эпигенетические изменения:
- Путь Wnt/β-catenin — регуляция пролиферации и дифференцировки.
- Путь PI3K/AKT/mTOR — метаболизм, рост, старение.
- Путь p53/p21 — клеточный цикл, апоптоз, старение.
- Путь NF-κB — воспаление, стресс-ответ.
Эпигенетический возраст отражает интегративное состояние этих процессов и считается биомаркером биологического старения, более точным, чем хронологический возраст.
Патофизиология
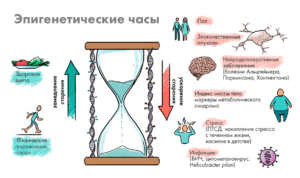
Повышенный эпигенетический возраст (т.е. старение быстрее нормы) ассоциирован с:
- Хроническими заболеваниями: сердечно-сосудистые болезни, сахарный диабет 2 типа, хроническая обструктивная болезнь лёгких (ХОБЛ), нейродегенеративные заболевания (например, болезнь Альцгеймера), некоторые виды рака.
- Факторами образа жизни: курение, ожирение, малоподвижность, хронический стресс, недостаток сна, нерациональное питание.
- Воспалением: Хроническое системное воспаление (inflammaging) коррелирует с ускоренным метилированием в определённых CpG-сайтах.
- Генетическими синдромами преждевременного старения: Прогерия (синдром Хатчинсона–Гилфорда), синдром Вернера — у этих пациентов эпигенетический возраст значительно превышает хронологический.
Механизмы связи:
- Накопление метильных изменений отражает клеточный стресс, окислительный дамаг ДНК, нарушение работы ДНК-метилтрансфераз (DNMTs) и деметилаз (TET-ферменты).
- Изменения метилирования в генах, связанных с воспалением, апоптозом и репарацией ДНК, способствуют функциональному ухудшению тканей.
- Модели, такие как GrimAge, напрямую включают CpG-сайты, предсказывающие уровни плазменных белков (например, GDF-15, TIMP-1), что усиливает связь с патофизиологией.
Сниженный эпигенетический возраст (молодящий эффект) наблюдается при:
- Долголетии (у центенаров).
- Интервенциях, замедляющих старение: калорийная рестрикция, физическая активность, приём метформина, NAD+-предшественников.
Референсные значения
Референсные значения зависят от:
- Используемой модели (Horvath, Hannum, PhenoAge, GrimAge и др.).
- Метода измерения (микрочипы, секвенирование).
- Биологического образца (кровь, слюна, ткани).
- Возраста и пола пациента.
Нормой считается соответствие эпигенетического возраста хронологическому или незначительное отклонение в пределах ±5 лет. Условно:
| Модель | Единицы измерения | Норма (отклонение от хронологического возраста) | Замечания |
|---|---|---|---|
| Horvath’s clock | лет | -5 до +5 лет | Универсальная модель, работает для разных тканей |
| Hannum’s clock | лет | -5 до +5 лет | Основана на крови, более чувствительна к возрастным изменениям в периферической крови |
| PhenoAge | лет | -5 до +5 лет | Коррелирует с фенотипическим старением и смертностью |
| GrimAge | лет | -5 до +5 лет | Наилучший прогноз смертности; значения >+5 лет — высокий риск |
Примечание: Абсолютные значения и границы нормы варьируются между лабораториями. Некоторые лаборатории предоставляют перцентили (например, 50-й перцентиль — средний биологический возраст для возраста/пола).
Методы определения
Основной метод — анализ метилирования ДНК с использованием микрочипов или секвенирования нового поколения (NGS).
- Infinium MethylationEPIC BeadChip (Illumina): наиболее распространённая платформа. Оценивает метилирование более чем в 850 000 CpG-сайтах. Высокая воспроизводимость, чувствительность — до 5% различий в метилировании.
- RRBS (Reduced Representation Bisulfite Sequencing): глубокое секвенирование CpG-богатых регионов после обработки ДНК бисульфитом. Высокая чувствительность, но дороже и сложнее в анализе.
- WGBS (Whole Genome Bisulfite Sequencing): полное картирование метилирования по всему геному. Наиболее точный, но очень дорогой и редко используется в рутинной практике.
Преаналитические требования:
- Образец: цельная кровь (в EDTA), слюна (в специальных пробирках, например, Oragene), сухие капли крови, биопсия ткани.
- Хранение: ДНК должна быть выделена в течение 24–72 часов после сбора крови; при хранении при -80 °C стабильна годами.
- Обработка бисульфитом: Ключевой этап — превращает неметилированный цитозин в урацил, в то время как метилированный цитозин остаётся неизменным. Позволяет различать модифицированные и немодифицированные участки.
ИФА, ИХЛА, ПЦР не используются для комплексного анализа эпигенетического возраста, но метилспецифичная ПЦР (MSP) или ПЦР в реальном времени после бисульфитной конверсии могут применяться для анализа отдельных CpG-сайтов.
Клинические показания
Когда назначают:
- Оценка биологического возраста у пациентов, интересующихся старением и профилактикой возраст-ассоциированных заболеваний.
- Мониторинг эффективности интервенций, направленных на замедление старения (образ жизни, нутрицевтики, фармакотерапия).
- Исследование в рамках клинических испытаний геропротекторов.
- Дифференциальная диагностика ускоренного старения (например, при синдромах преждевременного старения).
- Прогнозирование риска смертности и возраст-ассоциированных заболеваний (особенно по модели GrimAge).
Когда не назначают:
- Для рутинного скрининга в общей популяции без клинических показаний.
- Как единственный критерий для постановки диагноза или назначения терапии.
- Пациентам с острыми инфекциями или после недавнего хирургического вмешательства (возможны временные искажения).
- В педиатрической практике — модели валидированы в основном для взрослых.
Интерференции и ограничения
- Лекарства: Метформин, аспирин, статины, иммунодепрессанты могут модифицировать метильный профиль. Например, метформин ассоциирован с замедлением эпигенетического возраста.
- Онкологические заболевания: Рак может вызывать как ускорение, так и замедление эпигенетического возраста в зависимости от типа опухоли и ткани.
- Гематологические нарушения: Лейкоцитоз, лейкопения, анемии, трансплантация костного мозга — влияют на состав клеток крови, что искажает результаты (особенно для Hannum и PhenoAge).
- Временные факторы: Острая инфекция, травма, операция — могут временно ускорять эпигенетический возраст.
- Полиморфизмы ДНК: Генетические варианты в CpG-сайтах могут мешать гибридизации на микрочипах.
- Ограничения моделей: Не все модели одинаково точны для всех этнических групп. Большинство разработаны на когортах европейского происхождения.
Интерпретация и тактика
При отклонении в сторону ускоренного старения (эпигенетический возраст > хронологического на 5+ лет):
- Провести оценку факторов риска: образ жизни, метаболический статус, воспаление, сон, стресс.
- Назначить или оптимизировать терапию: контроль АД, гликемии, липидов, ИМТ.
- Рекомендовать изменения образа жизни: физическая активность (150 мин/нед умеренной интенсивности), сбалансированное питание (Mediterranean diet), отказ от курения, нормализация сна.
- Рассмотреть применение геропротекторов (в рамках клинических исследований или при наличии показаний): метформин, NAD+-предшественники (никотинамид рибозид), ресвератрол.
- Планировать повторный тест через 12–24 месяца для оценки динамики.
Целевые значения при терапии: Цель — снизить разницу между эпигенетическим и хронологическим возрастом до пределов нормы (±5 лет) или достичь стабилизации/замедления темпов старения.
Советы пациенту: Эпигенетический возраст — это отражение воздействия образа жизни и окружающей среды. Он обратим. Изменения в питании, движении и сне могут положительно повлиять на метильный профиль. Однако тест не является диагнозом и должен интерпретироваться в контексте общего клинического статуса.
Связь с другими маркерами
Эпигенетический возраст интерпретируют в комплексе с другими биомаркерами старения и риска:
- Теломерная длина: Альтернативный маркер клеточного старения. Слабая корреляция с метилированием ДНК — отражают разные аспекты старения.
- Инflammatory markers: IL-6, TNF-α, hs-CRP — повышены при ускоренном эпигенетическом возрасте.
- Метаболические маркеры: инсулин, HOMA-IR, лептин, адипонектин — связаны с метилированием в генах, регулирующих метаболизм.
- Функциональные тесты: VO2max, когнитивные тесты, сила хвата — коррелируют с PhenoAge и GrimAge.
- Клинические шкалы: Физическая и когнитивная фрилитетность, индекс коморбидности.
Модель GrimAge уже включает предсказанные уровни белков (например, TIMP-1, GDF-15), что делает её частично интегрированной с протеомными данными.
Вывод
Эпигенетический возраст по метилированию ДНК — это объективный биомаркер биологического старения, основанный на систематических изменениях метильного профиля генома. Он отражает влияние генетики, образа жизни и болезней, превосходя хронологический возраст в прогнозировании риска смертности и возраст-ассоциированных патологий. Анализ проводится с помощью микрочипов или NGS после бисульфитной конверсии ДНК из крови, слюны или тканей. Интерпретация требует учёта модели (Horvath, GrimAge и др.), метода и клинического контекста. Ускорение эпигенетического возраста обратимо и может корректироваться через изменения образа жизни и, потенциально, фармакологические интервенции. Тест остаётся в основном исследовательским инструментом, но постепенно входит в клиническую практику превентивной и антивозрастной медицины.

