Идентификация и биохимия
Анализ «Микробиота кала» не является определением одного конкретного биомаркера, а представляет собой комплексное исследование сообщества микроорганизмов, обитающих в толстом кишечнике, с использованием молекулярно-генетических методов. Основными методами являются секвенирование гена 16S рРНК (рибосомной РНК) и шотган-метагеномное секвенирование (shotgun metagenomics).
Полное название: Анализ состава микробиоты кала методом секвенирования 16S рРНК или шотган-метагеномики.
Синонимы: Микробиом кишечника, кишечная микробиота, метагеномный анализ кала, профилирование микробиоты, анализ микробиоценоза кишечника.
Мишень анализа: Рибосомная РНК бактерий (16S рРНК) или полногеномная ДНК микробных сообществ.
Ген: 16S рРНК кодируется геном rrs (16S рибосомальной РНК), присутствующим во всех прокариотах. В шотган-подходе анализируются все гены, присутствующие в ДНК образца.
Молекулярная масса и форма: Анализируется не белок и не метаболит, а нуклеиновые кислоты (ДНК). Молекулярная масса ДНК варьируется в зависимости от вида микроорганизма и количества амплифицированных фрагментов. Для 16S рРНК типичный амплифицируемый фрагмент составляет 300–500 пар оснований.
LOINC-код: LOINC-код может отличаться в зависимости от лаборатории, метода и уровня детализации. Примерные коды: 94330-7 (Microbiome of Stool by Sequencing), 78855-8 (16S ribosomal RNA gene Sequencing of Stool). Точные коды зависят от конкретного протокола и должны уточняться в лаборатории.
SNOMED CT: SNOMED-коды также варьируются. Пример: 710905005 (Finding of microbial flora of feces), 252180004 (Analysis of specimen from feces). Унифицированный код для метагеномного анализа микробиоты в SNOMED отсутствует.
Физиологическая роль
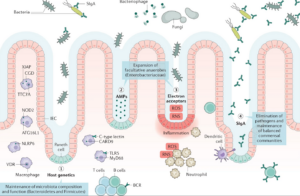
Кишечная микробиота — это сложное сообщество бактерий, архей, грибов и вирусов, населяющих просвет толстого кишечника. Основные представители — бактерии из фил Firmicutes, Bacteroidetes, Actinobacteria, Proteobacteria и Verrucomicrobia.
Микробиота вырабатывается и поддерживается в толстом кишечнике, хотя небольшие популяции присутствуют и в других отделах ЖКТ. Её формирование начинается при рождении и продолжается в первые 2–3 года жизни, после чего достигает относительной стабильности.
Ключевые физиологические функции микробиоты:
- Ферментация неперевариваемых углеводов: Микроорганизмы расщепляют диетические волокна до короткоцепочечных жирных кислот (КЦЖК), таких как ацетат, пропионат и бутират. Бутират служит основным источником энергии для колоноцитов и обладает противовоспалительными свойствами.
- Модуляция иммунной системы: Микробиота взаимодействует с иммунными клетками слизистой оболочки кишечника, способствуя дифференцировке регуляторных Т-клеток (Treg), снижая воспаление и поддерживая толерантность к пищевым антигенам.
- Синтез витаминов: Некоторые виды синтезируют витамины группы B (B12, фолиевая кислота) и витамин K.
- Защита от патогенов: Механизмы включают конкурентное исключение, выработку антимикробных пептидов (бактериоцинов) и поддержание низкого pH за счёт КЦЖК.
- Метаболизм желчных кислот: Микробиота превращает первичные желчные кислоты в вторичные (например, хенодезоксихолевая → литохолевая), что влияет на липидный обмен и сигнализацию через рецепторы FXR и TGR5.
- Влияние на центральную нервную систему: Через кишечник-мозговую ось (gut-brain axis) микробиота участвует в регуляции настроения, тревожности и когнитивных функций через нервные, эндокринные и иммунные пути.
Патофизиология
Нарушение состава и функции микробиоты — дисбиоз — связано с множеством заболеваний. Дисбиоз характеризуется снижением микробного разнообразия, изменением соотношения ключевых таксонов и потерей функциональной устойчивости экосистемы.
Состояния, ассоциированные с дисбиозом:
- Воспалительные заболевания кишечника (ВЗК): Язвенный колит и болезнь Крона связаны со снижением Firmicutes (особенно Faecalibacterium prausnitzii, продуцирующего бутират) и увеличением Proteobacteria (включая потенциально патогенные энтеробактерии).
- Синдром раздражённого кишечника (СРК): Отмечаются изменения в относительном содержании Bifidobacterium, Lactobacillus, Ruminococcus, а также повышенное количество метаногенных архей (Methanobrevibacter smithii) при запорах.
- Ожирение и метаболический синдром: Увеличение отношения Firmicutes/Bacteroidetes в некоторых исследованиях ассоциировано с ожирением, хотя данные противоречивы. Также важна функциональная активность микробиоты — например, способность извлекать энергию из пищи.
- Тип 2 сахарный диабет: Наблюдается снижение продуцентов бутирата и увеличение условно-патогенных видов.
- Аутоиммунные заболевания: Рассеянный склероз, ревматоидный артрит, системная красная волчанка — все они связаны с нарушением микробиоты и повышенной проницаемостью кишечного барьера («синдром течёжелого кишечника»).
- Психические расстройства: Депрессия, тревожные расстройства, аутизм — при этих состояниях выявляются характерные сдвиги в микробиоте, включая снижение Bifidobacterium и Lactobacillus.
- Аллергии и атопические заболевания: Ранняя дестабилизация микробиоты (например, после антибиотиков) может нарушить формирование иммунной толерантности.
Механизмы связи включают: нарушение барьерной функции кишечника, системное воспаление, изменение метаболизма нейромедиаторов (серотонин, ГАМК, дофаминДофамин – это нейромедиатор и гормон, играющий ключевую роль в системе вознаграждения мозга, мотивации, удовольствии, обучении и регуляции движений. Основные функции: Стимулирует чувство удовольствия и удовлетворения. Участвует в процессах мотивации и принятия решений. Регулирует двигательную активность. Влияет на память, внимание и настроение.), модуляцию иммунного ответа и нарушение метаболизма желчных кислот.
Референсные значения
Референсные значения для микробиоты кала не унифицированы и зависят от метода (16S рРНК vs шотган), региона, диеты, возраста, пола и этнической принадлежности. Ниже приведена обобщённая таблица, отражающая типичные характеристики «здоровой» микробиоты у взрослых.
| Показатель | Референсное значение (взрослые) | Единицы измерения | Замечания |
|---|---|---|---|
| Микробное альфа-разнообразие (Shannon index) | 3,0 – 4,5 | Безразмерный индекс | Зависит от метода и популяции; снижено при ВЗК, СРК, ожирении |
| Соотношение Firmicutes / Bacteroidetes | 0,5 – 1,5 | Отношение | Высокая вариабельность между людьми; не является надёжным маркером сама по себе |
| Доля Firmicutes | 40 – 60 % | % от общей микробиоты | Включает Clostridiales, Lactobacillales, Bacillales |
| Доля Bacteroidetes | 30 – 50 % | % от общей микробиоты | Включает Bacteroides, Prevotella |
| Доля Actinobacteria | 1 – 10 % | % от общей микробиоты | Включает Bifidobacterium |
| Доля Proteobacteria | < 5 % | % от общей микробиоты | Повышение — маркер дисбиоза (например, при ВЗК) |
| Наличие Faecalibacterium prausnitzii | Выявляется у > 95 % здоровых | Относительная доля | Снижение — маркер воспаления |
Зависимость от возраста: У новорождённых преобладают Proteobacteria и Actinobacteria (включая Bifidobacterium), к 3 годам формируется «взрослый» профиль. У пожилых лиц наблюдается снижение разнообразия и увеличение Proteobacteria.
Пол: Некоторые исследования показывают небольшие различия в составе микробиоты у мужчин и женщин, но клиническая значимость не установлена.
Методы определения
Основные методы анализа микробиоты кала:
- Секвенирование 16S рРНК:
- Принцип: Амплификация гипервариабельных регионов гена 16S рРНК (например, V3-V4) с последующим высокопроизводительным секвенированием (NGS).
- Разрешение: До уровня рода, редко — вида.
- Преимущества: Низкая стоимость, достаточная для оценки структуры сообщества.
- Недостатки: Не позволяет оценить функциональные возможности микробиоты, возможны артефакты при амплификации.
- Чувствительность: Обнаруживает микроорганизмы при содержании > 0,1 % от общей биомассы.
- Платформы: Illumina MiSeq, NextSeq.
- Шотган-метагеномное секвенирование (shotgun metagenomics):
- Принцип: Прямое секвенирование всей ДНК образца без амплификации.
- Разрешение: До уровня штамма, позволяет идентифицировать виды и гены.
- Преимущества: Полная характеристика таксономического состава и функционального потенциала (например, гены, участвующие в синтезе КЦЖК).
- Недостатки: Высокая стоимость, большие объёмы данных, требует биоинформатической обработки.
- Чувствительность: Может выявлять микроорганизмы при содержании < 0,01 %.
- Платформы: Illumina NovaSeq, Oxford Nanopore (редко).
- Прочие методы: ПЦР в реальном времени (для отдельных видов), культуральные методы (ограничены, так как ~80 % кишечных бактерий не культивируются), метатранскриптомика (анализ РНК — функциональная активность).
Преаналитические требования:
- Сбор образца — в стерильный контейнер, без консервантов или с ними (в зависимости от набора).
- Хранение: немедленное замораживание при –80 °C или использование стабилизаторов (например, OMNIgene•GUT).
- Транспортировка: при комнатной температуре (со стабилизатором) или замороженным.
- Избегать загрязнения мочой, водой, туалетной бумагой.
- Пациент должен избегать антибиотиков минимум 4 недели до анализа (если возможно).
Клинические показания
Когда назначают:
- Диагностика и мониторинг воспалительных заболеваний кишечника (ВЗК), особенно при неясной этиологии.
- Оценка дисбиоза у пациентов с синдромом раздражённого кишечника (СРК).
- Исследование причин рецидивирующего дисбактериоза или постинфекционного синдрома.
- Оценка состояния микробиоты перед и после фекальной трансплантации (FMT).
- Исследование связи микробиоты с метаболическими, неврологическими или аутоиммунными заболеваниями в рамках научных или комплексных обследований.
- Контроль эффективности пробиотиков, пребиотиков или диетотерапии (например, низкоферментируемая диета при СРК).
Когда не назначают:
- Для скрининга в общей популяции (отсутствие доказанной клинической пользы).
- Как единственный метод диагностики инфекций ЖКТ (для этого используют ПЦР-панели на патогены).
- При острых инфекциях кишечника (например, сальмонеллёз, клостридиоидная инфекция) — требуется специфическое тестирование.
- Для подтверждения «токсичности» или «засорения кишечника» — термины не имеют научной основы.
Интерференции и ограничения
Лекарства:
- Антибиотики: Резко изменяют состав микробиоты, снижают разнообразие. Интерпретация невозможна в течение 4–8 недель после приёма.
- Пробиотики: Могут временно увеличивать долю определённых штаммов (например, Lactobacillus, Bifidobacterium), что может исказить «базовый» профиль.
- Пребиотики, диетические добавки: Влияют на рост определённых бактерий.
- Ингибиторы протонной помпы (ИПП): Ассоциированы с увеличением Proteobacteria.
- Метформин: Меняет микробиоту, увеличивая Escherichia и Akkermansia.
Биологические факторы:
- Диета: Высокое содержание клетчатки — увеличивает разнообразие; животный жир и сахар — снижают. Вегетарианская и средиземноморская диеты ассоциированы с более благоприятным профилем.
- Физическая активность: Связана с увеличением разнообразия.
- Хронический стресс: Может снижать Lactobacillus и Bifidobacterium.
Ложные результаты:
- Загрязнение образца (вода, моча) — может привести к снижению концентрации ДНК и артефактам.
- Неправильное хранение — деградация ДНК, особенно без стабилизатора.
- Биоинформатические ошибки — неправильная классификация таксонов, особенно при использовании неполных баз данных.
- Межлабораторная вариабельность — различия в протоколах выделения ДНК, секвенировании и анализе.
Интерпретация и тактика
Интерпретация результатов должна проводиться в контексте клинической картины, анамнеза и других анализов. Отклонения включают:
- Снижение альфа-разнообразия: Ассоциировано с хроническими заболеваниями. Цель терапии — его восстановление (диета, пребиотики, FMT).
- Повышение Proteobacteria: Маркер дисбиоза и воспаления. Требует поиска причины (антибиотики, воспаление, диета).
- Снижение Faecalibacterium prausnitzii: Связано с ВЗК. Возможна коррекция пребиотиками (инулин, ФОС) или FMT.
- Повышение Akkermansia muciniphila: В большинстве исследований — благоприятный маркер (улучшение барьерной функции), но может повышаться и при воспалении.
Целевые значения при терапии: Увеличение альфа-разнообразия (Shannon > 3,5), снижение доли Proteobacteria до < 5 %, восстановление F. prausnitzii.
Советы пациенту:
- Избегайте ненужных антибиотиков.
- Увеличьте потребление пищевых волокон (овощи, фрукты, цельнозерновые).
- Рассмотрите включение ферментированных продуктов (кефир, квашеная капуста, темпе).
- Соблюдайте режим питания, избегайте переедания и стрессов.
- Не интерпретируйте результаты изолированно — обсуждайте их с врачом.
Связь с другими маркерами
Анализ микробиоты кала интерпретируется в сочетании с:
- Калом на скрытую кровь (FIT): Исключение колоректального рака или ВЗК.
- Кал на кальпротектин: Маркер кишечного воспаления. Повышен при ВЗК, может быть нормальным при СРК.
- Панель на патогены кишечника (ПЦР): Выявление Salmonella, Shigella, Campylobacter, Clostridioides difficile.
- Биохимия крови: С-реактивный белок, СЧТ, альбуминОдин из основных белков человеческого организма, который отвечает за поддержание нормального состава крови и транспортировку различных веществ по организму. Он также выступает запасным источником аминокислот Альбумины выполняют две очень важные функции: управляют распределением воды внутри организма,
помогают крови переносить витамины, минералы и лекарства.
Они отвечают за обмен воды — помогают удерживать её в сосудах и не позволяют ей избыточно переходить в ткани (таким образом предотвращая развитие отёков). Альбумины влияют н — для оценки системного воспаления и питания. - Маркеры проницаемости кишечника: Зонулин, L-лактат (в исследовательских целях).
- Метаболом кала: Анализ КЦЖК — функциональное подтверждение активности микробиоты.
Вывод
Анализ микробиоты кала методом 16S рРНК или шотган-метагеномики позволяет оценить состав и разнообразие кишечного микробиоценоза. Это исследование не является рутинным, но имеет ценность при диагностике и мониторинге ВЗК, СРК, после антибиотикотерапии и при подготовке к FMT. Референсные значения зависят от метода, популяции и лаборатории. Интерпретация требует учёта диеты, лекарств и клинической картины. Дисбиоз характеризуется снижением разнообразия, изменением соотношения фил и потерей ключевых антивоспалительных видов. Метод имеет ограничения, включая преаналитические ошибки и интерференцию лекарств. Результаты следует интегрировать с другими маркерами воспаления и функции кишечника.

